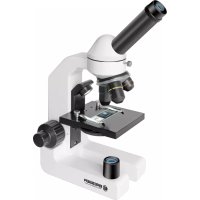
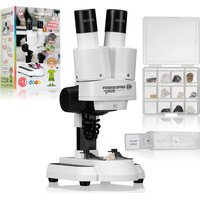
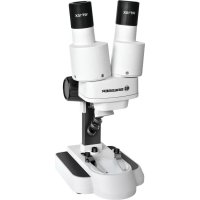
BIODISCOVER 201280X - Microscopio BRESSER - Manual de uso y guía de instrucciones gratis
Encuentra gratis el manual del aparato BIODISCOVER 201280X BRESSER en formato PDF.

Preguntas frecuentes - BIODISCOVER 201280X BRESSER
Preguntas de los usuarios sobre BIODISCOVER 201280X BRESSER
0 pregunta sobre este aparato. Responde a las que conoces o haz la tuya.
Hacer una nueva pregunta sobre este aparato
Descarga las instrucciones para tu Microscopio en formato PDF gratis! Encuentra tus instrucciones BIODISCOVER 201280X - BRESSER y toma tu dispositivo electrónico nuevamente en la mano. En esta página están publicados todos los documentos necesarios para el uso de su dispositivo. BIODISCOVER 201280X de la marca BRESSER.
MANUAL DE USUARIO BIODISCOVER 201280X BRESSER
La utilización de este dispositivo suele requerir el empleo de herramientas puntiagudas o de bordes afilados, lo que significa que deberá guardar éste y todos sus accesorios y elementos adicionales en un lugar alejado del alcance de los niños. No deje que los niños manipulen el aparato, a menos que se encuentren bajo supervisión de un adulto. Asimismo, mantenga el material de embalaje (bolsas de plástico, bandas de goma, etc.) lejos del alcance de los niños.
A

BRESSER®

text_image
A WF 10X WF 5X WF 16X 17 16 15 14 13 12 11 10 WF5X BRESSER Bioliviscover- B BRESSE
② Ocular WF5x de gran campo
3 Lente Barlow
4 Tubo portaoculares
5 Cabezal monocular del microscopio
⑥ Iluminación por LED (incidente)
7 Rueda de enfoque
8 Regulador de intensidad de luz/interruptor On/Off
9 Alimentación de corriente
10 Hueco para oculares
⑪ Combinación de filtros de colores y rueda del diafragma
⑫ Iluminación por LED (transmitida)
13 Platina
14Pinzas
15 Objetivos
17 Tornillo de ajuste del cabezal
Componentes (Fig. B):
18 Cuchilla cilíndrica para la preparación de muestras (Microtomo)
19 Pinzas
20 Pipeta
21 Agujas para preparaciones
22 Recipiente para la incubación
23 Levadura
24 "Gum media"
25 Sal marina
26 Huevos de gamba
27 Caja con muestras preparadas, portas y cubres en blanco
28 Adaptador de corriente
29 Carro móvil (opcional)
30 Tornillo regulador de altura máxima de platina
31 Ajuste longitudinal
32 Ajuste transversal
Índice Página
- General/Situación
- Iluminación por LED 15
- Filtros de combinación de colores y rueda del diafragma 15
- Ajustes del microscopio (iluminación transmitida) 15
- Observación 15
- Observación de muestras – Características y preparación 16
- Ajustes del microscopio (luz incidente) 16
- Experimentos (luz transmitida) 16
- Accesorios opcionales 17
- Cuidados y mantenimiento 17
- Datos técnicos 18
- Declaración de conformidad con la UE 18
Garantía y servicio 19
Nota importante:
Estas instrucciones incluyen una página desplegable al principio y otra final con figuras numeradas. Esto hace que las instrucciones sean más facil de entender. Todas las figuras numeradas con el prefijo A hacen referencia a las figuras del primer desplegable y las del prefijo B a las que se encuentran en el desplegable del final.
1. General/Situación
Antes de comenzar a utilizar su microscopio, elija una ubicación adecuada. Asegúrese que descansa sobre una superficie estable libre de vibraciones.
La utilización de la iluminación eléctrica requiere una conexión (220-230V). (Por razones de seguridad, utilice sólo el adaptador de corriente suministrado. Otros adaptadores pueden no cumplir con las especificaciones técnicas. No nos hacemos responsables de ningún daño causado por la utilización de otros adaptadores).
2. Iluminación por LED
El microscopio tiene dos unidades independientes de iluminación regulables que se controlan mediante potenciómetros (Fig. A 8). La iluminación transmitida se utiliza para muestras transparentes. Para observar muestras sólidas que no son transparentes, utilice la iluminación incidente, y para muestras semi-transparentes, utilice simultáneamente la luz incidente y transmitida. Este modo no es recomendable para muestras transparentes, ya que puede reflejar en la muestra.
3. Filtros de combinación de colores y rueda del diafragma
Para ajustar la calidad de observación de muestras transparentes, utilice la rueda situada bajo la platina del microscopio (Fig. A 11). Dependiendo del color del filtro seleccionado, se podrán observar mejor los detalles de la muestra. En observaciones con luz incidente, por ejemplo con muestras transparentes, la luz transmitida coloreada en combinación con la incidente, mejorarán los detalles de la imagen. Dependiendo de la apertura del diafragma, utilice una intensidad de luz adecuada para mejorar el enfoque, contraste y la resolución de los detalles.
4. Ajustes del microscopio (iluminación transmitida)
Para realizar la primera observación hay que realizar ajustes en el microscopio (Fig. A 1-5). Primero, afloje el tornillo (Fig. A 17) y gire el cabezal (Fig. A 4) hasta conseguir una posición adecuada para realizar las observaciones. Ahora mire a través de los oculares, siempre empezando por el menor aumento. Desplace la platina del microscopio (Fig. A 13) hacia abajo utilizando el mando de enfoque (Fig. A 7) y gire el revólver (Fig. A 16) hasta el objetivo de menor aumento (4x). (Ahora el objetivo de 4x está colocado verticalmente hacia abajo).
Inserte el ocular de 5x (Fig. A 2) dentro de la lente Barlow (Fig. A 3). Asegúrese que la lente Barlow se encuentra totalmente dentro del tubo portaoculares (Fig. A 4) y que no sobresalga hacia fuera.
Nota:
Antes de cambiar de objetivo, siempre desplace la platina del microscopio hacia abajo. Esto evita posibles daños.
5. Observación
Cuando haya preparado el microscopio con su correspondiente iluminación, deberá tener en cuenta lo siguiente:
- Comience todas las sesiones de observación con el menor número de aumentos (ocular 5x y objetivo 4x). De este modo, es más fácil de realizar el centrado y enfoque del objeto.
- Cuanto mayor sea el número de aumentos, mayor será la intensidad de luz necesaria para poder obtener una buena calidad de imagen.
Coloque una muestra bajo el objetivo del microscopio y fijela con las pinzas (Fig. A 14).
Importante: La muestra debe estar colocada en el centro de la luz transmitida.
Ahora mire a través del ocular (Fig. A 1/2) y gire el mando de enfoque (Fig. A 7) cuidadosamente hasta que observe la imagen enfocada. Utilice el potenciómetro (Fig. A 8) para regular la intensidad de la luz transmitida y poder observar los detalles de la muestra adecuadamente. Puede obtener mayores aumentos desplazando la lente Barlow (Fig. A 3) cuidadosamente fuera del tubo portaocular (Fig. A 4). Cuando la lente Barlow está casi fuera, el aumento es casi el doble.
Para conseguir mayores aumentos, utilice el ocular de 16x (Fig. A 1) y luego gire el revolver (Fig. A 16) a un mayor objetivo (10x/40x).
Nota Importante:
Mayores aumentos no implican mejores resultados. Esto depende de la muestra.
Tenga en cuenta:
Al cambiar el nivel de ampliación (cambio de ocular o de objetivo o extracción de lente Barlow) deberá volver a utilizar el mando de enfoque (Fig. A 7) para recuperar la nitidez de la imagen. Sea cuidadoso al realizar el ajuste. Si eleva la platina del microscopio con demasiada rapidez, el objetivo y el portaobjetos pueden entrar en contacto y sufrir daños.
6. Observación de muestras – Características y preparación
6.1 Condiciones
Con este microscopio que presenta luz incidente y transmitida se pueden realizar observaciones con muestras transparentes y opacas. Si se observan muestras opacas; como pequeños animales, partes de plantas, tejidos, piedras, etc; la luz incidente (desde arriba) es reflejada sobre la muestra y pasa a través del objetivo y ocular, donde la imagen es aumentada, y nos llega hasta al ojo.
Si se realizan observaciones con muestras transparentes, la luz transmitida (desde abajo) atraviesa la muestra, el objetivo y el ocular hasta llegar al ojo.
Muchos de los microorganismos del agua, componentes de plantas y pequeñas partes de animales, que por naturaleza tienen la característica de ser transparentes, no hacen falta prepararlos antes de la observación; mientras que otros deben prepararse según corresponda. En el caso de tener que convertir muestras opacas en trasparentes hay que realizar un pretratamiento o la inyección de sustancias (fluidos) adecuadas transparentes o se recortan láminas extremadamente finas de los mismos (manualmente o con un microtomo) para observarlas a continuación.
6.2 Preparación de cultivos
Como ya hemos mencionado antes, en primer lugar es necesario obtener segmentos del objeto a observar lo más finos posible. Para obtener resultados óptimos, necesitaremos un poco de cera o parafina. Si el equipo del microscopio no incluye este tipo de material, puede utilizar una vela normal. Introduzca la cera en un recipiente y caliéntelo con una llama. Ahora sumerja el objeto varias veces en la cera ya fundida y después, espere a que la cera se seque y se endurezca. Utilice un microtomo (Fig. B 18), un cuchillo/escalpelo (¡¡tenga cuidado!!) o cualquier instrumento cortante adecuado para obtener láminas lo más finas posible del objeto que está recubierto con la cera. Por último, coloque estas láminas del objeto sobre el portaobjetos y tápelos con un cubreobjetos.
6.3 Elaboración de un cultivo propio
Coloque el objeto que vaya a observar en un portaobjetos de vidrio y utilice una pipeta (Fig. B 20) para verter una gota de agua destilada sobre dicho objeto (Fig. B I). A continuación, coloque un cubreobjetos en sentido perpendicular al borde de la gota de agua, de modo que éste transcurra a lo largo del borde del cubreobjetos (Fig. B II). Ahora baje lentamente el cubreobjetos sobre la gota de agua.
Nota:
El “Gum media” proporcionado (Fig. B 24) se utiliza para fabricar preparados permanentes. Use éste en vez de agua destilada. El “Gum media” se endurece, por lo que el objeto se fija de forma permanente en el portaobjetos.
7. Ajustes del microscopio (luz incidente)
Para iluminar correctamente cualquier muestra, usted puede regular la intensidad de luz incidente y transmitida a la vez o individualmente. Los mejores resultados utilizando el modo de luz incidente se consiguen combinando el ocular de 5x y el objetivo de 4x. Cualquier otra combinación incrementa los aumentos, pero reduce el campo visual.
8. Experimentos (luz transmitida)
Una vez que se haya familiarizado con su microscopio podrá realizar los siguientes experimentos:
8.1 Impresiones de periódicos
Objetos:
- Pequeño pedazo de papel de periódico que contenga partes de una ilustración y algunas letras.
- Un pedazo de papel similar al anterior procedente de una revista.
Para poder observar las letras y las imágenes, elabore de cada objeto un cultivo limitado temporalmente.
Ajuste su microscopio al menor aumento y utilice el cultivo elaborado con el periódico. Las letras se verán deshilachadas y rasgadas, porque el periódico se imprime sobre papel bruto de baja calidad. Sin embargo, las letras de las revistas se observarán lisas y continuas.
La imagen del periódico se verá como un conjunto de muchos puntos pequeños, que aparecerán algo sucios; mientras que los puntos de la imagen de la revista (puntos de trama) serán mucho más nítidos.
8.2 Fibras textiles
Objetos y accesorios:
- Hilos de diversos tejidos: algodón, lino, lana, seda, rayón, nylon, etc.
- Dos agujas.
Coloque cada hilo en un portaobjetos de vidrio y únalos con ayuda de dos agujas. Humedezca los hilos y cúbralos con un cubreobjetos. A continuación, ajuste el microscopio al menor aumento.
-Lasfibras de algodón son de origen vegetal y se ven a través del microscopio como una banda plana y retorcida. Las fibras son más gruesas y redondas en los bordes que en el centro.
Las fibras de algodón parecen tubitos largos y contraídos.
-Lasfibras de lino también tienen origen vegetal, son redondas y transcurren en línea recta. Brillan como la seda y muestran numerosos abultamientos en el filamento de la fibra.
-Laseda es de origen animal y consta de una cantidad masiva de fibras de pequeño diámetro, lo que las diferencia de las fibras vegetales huecas. Cada fibra es lisa y homogénea, y tiene el aspecto de un pequeño bastoncillo de vidrio.
- Las fibras de lana son de origen animal y la superficie consta de cápsulas solapadas que aparecen discontinuas y onduladas.
Si es posible, compare las fibras de algodón de diversos tejidos y observe el diferente aspecto que éstas presentan. Los expertos pueden deducir a partir de este hecho, el país de origen del tejido.
- El rayón tiene un origen sintético y se fabrica mediante un largo proceso químico. Todas las fibras muestran líneas duras y oscuras sobre una superficie lisa y brillante. Las fibras se rizan después de secarse en las mismas condiciones. Observe las similitudes y las diferencias.
8.3 ¿Cómo se desarrolla el moho en el pan?
Objeto: Un pedazo de pan duro.
Las esporas de los hongos, los cuales crecen en nuestro pan, se encuentran por toda la atmósfera.
Coloque el pan en un portaobjetos y pulverice un poco de agua por encima. Simplemente humedezca el pan, no lo empape.
Introduzca el conjunto en un recipiente con cierre de rosca y guárdelo
en un armario en el que entre poca luz y la temperatura sea templada. En muy poco tiempo aparecerá el moho en el pan. Observe el pan todos los días.
En la primera fase del moho, aparecerá una pelusa blanca y brillante. Colóquelo en un portaobjetos para observarlo. El material está representado por una masa de hilos entrelazados que forman en conjunto el cuerpo del hongo. Cada hilo es una hifa, y todo el conjunto recibe el nombre de Micelio.
Poco después aparecerán algunos rizoides que unen el hongo del moho con el pan, y de este modo obtienen agua y nutrientes que permiten que el micelio pueda seguir creciendo. Los rizoides irán adoptando un color marrón a medida que pase más tiempo.
En sentido vertical a este grupo crecen hifas (tallos largos y delgados), que terminan en una diminuta esfera blanca. Este tallo recibe el nombre de esporangióforo (portador de la cápsula de la espora), mientras que la esfera es un esporangium o una cápsula de esporas. Poco después estas esferas adoptan un color negro. Además, las esporas que se encuentran en el interior maduran.
Cuando la cápsula de esporas se abre, las esporas se liberan, pasanal aire y pueden infectar a otro pan. A simple vista, las cápsulas de esporas se reconocen como diminutas manchas negras. Están dispersadas en la superficie del moho y con ello, dan su nombre al moho. Pueden ser de color rosa, rojo, azul o verde.
Usted puede crear cultivos de todos los estadios del moho del pan.
8.4 Gambas de agua salada
Accesorios:
- Levadura (Fig. B 23)
- "Gum Media" (Fig. B 24)
- Sal marina (Fig. B 25)
- Huevos de gamba (Fig. B 26)
- Recipiente para la incubación de huevos de gamba (Fig. B 22)
8.4.1 Ciclo vital de las gambas de agua salada
La gamba de agua salada, también conocida por los científicos como “Artimia Salina”, tiene un peculiar e interesante ciclo vital. Los huevos, producidos por las hembras, se encuban sin que hayan sido jamás fecundados por una gamba macho. Todas las gambas que surgen de esos huevos encubados son hembras. En casos extraordinarios, podrían surgir de estos huevos alguna gamba macho. Estos machos fecundan los huevos de las hembras y del apareamiento surgen huevos especiales. Estos huevos, llamados “huevos de invierno” tienen un grueso caparazón de protección. Los huevos de invierno son muy resistentes e incluso siguen vivos cuando se quedan sin agua. Pueden incluso persistir en este estado “durmiente” entre 5 y 10 años. Los huevos se encuban cuando se vuelvan a dar las condiciones medioambientales adecuadas. Los huevos incluidos (Fig. B 26) son de este tipo.
8.4.2 Incubación de las gambas de agua salada
Para incubar las gambas, primero es necesario producir una solución salina que se corresponda con las condiciones de vida de las gambas. Llene un recipiente con medio litro de agua de lluvia o de grifo. Deje reposar éste agua aproximadamente 30 horas. Como durante este período de tiempo el agua se evapora, es aconsejable rellenar un segundo recipiente y dejarlo reposar 36 horas. Una vez pasado este tiempo, vacía la mitad de la sal marina que le adjuntamos (Fig. B 25) en el recipiente y remuévalo hasta que la sal se haya disuelto. Añada un poco del agua marina que se ha producido, en el recipiente de incubación de gambas (Fig. B 22). Coloque ahora algunos de los huevos y cierre la tapa. Coloque la instalación en un lugar iluminado, pero evite exponer el recipiente a la luz directa del sol. Tendría que estar a una temperatura de aprox. 25°C. A esta temperatura y tras 2-3 días aproximadamente, la gamba sale del huevo. Si durante este período de tiempo el agua del recipiente se evapora, añada agua del segundo recipiente.
8.4.3 Las gambas de agua salada bajo el microscopio El animal que sale del huevo es conocido bajo el nombre de "Nauplio". Con ayuda de la pipeta (Fig. B 20), coloque unas cuantas de esas larvas en un portaobjetos de vidrio y observe. La larva se desplaza por la solución salina con ayuda de sus protuberancias capilares. Saque diariamente una larva del recipiente y obsérvela en el microscopio. Si cada día contempla las larvas a través del microocular y además almacena las imágenes así conseguidas, obtendrá una documentación fotográfica ininterrumpida y completa del ciclo vital de las gambas de agua salada. Si lo desea también puede sacar la tapa superior del recipiente de incubación de gambas y colóquelo entero en la platina. Dependiendo de la temperatura ambiental, la larva estará ya madura en un plazo de 6 a 10 semanas. Pronto habrá cultivado una generación completa de gambas de agua salada que se reproducen constantemente.
8.4.4 Alimentación de las gambas de agua salada
Para mantener con vida las gambas de agua salada, tiene que alimentarlas de vez en cuando. Esto tiene que hacerse con mucho cuidado, porque en caso de sobrealimentación, el agua se pudre y nuestra población de gambas se envenena. La alimentación se efectúa preferentemente con levadura seca en polvo (Fig. B 23). De a las gambas un poco de esa levadura cada dos días. Si el agua del recipiente de incubación se pone oscura, es que se está pudriendo. En ese caso, saque las gambas inmediatamente del agua y métalas en otra solución salina recién hecha.

text_image
Atención: ¡Ni los huevos de gamba ni las gambas en sí son aptas para el consumo!9. Accesorios opcionales
Como accesorio opcional para el Bresser BioDiscover hay disponible un carro móvil (Fig. B 29). Extraiga las pinzas para poderlo instalar (Fig. A 14). Utilice el tonillo (Fig. B 30) para sujetar el carro móvil a la platina del microscopio. Utilice los tornillos de ajuste (Fig. B 31+32) para ajustar la muestra longitudinalmente (Fig. B 31) y transversalmente (Fig. B 32).
10. Cuidados y mantenimiento
Su microscopio es un dispositivo óptico de alta calidad. Por lo tanto, evite que entre en contacto con polvo o humedad.
No toque ninguna superficie óptica con los dedos.
Si a pesar de todo, el microscopio o los accesorios tienen rastros de polvo o humedad, retírelos con un cepillo suave.
A continuación, limpie la superficie afectada con un paño suave y sin desgastar.
Para limpiar las huellas de dedos de las superficies ópticas, utilice un paño suave y sin desgastar ligeramente humedecido en alcohol.
Después de terminar de utilizar el microscopio y sus accesorios, debe volver a colocarlos en sus correspondientes fundas.
Recuerde: Un buen mantenimiento y cuidado del microscopio conservasu calidad óptica durante años, y por lo tanto, mantiene su valor.
11. Datos técnicos
Tabla de aumentos
| Ocular | Objetivo | Aumento | Con lente | Barlow |
| 5x | 4x | 20x | ||
| 5x | 10x | 50x | 100x | |
| 5x | 40x | 200x | 400x | |
| 16x | 4x | 64x | ||
| 16x | 10x | 160x | ||
| 16x | 40x | 640x |
12. Declaración de conformidad con la UE
Bresser GmbH, con sede en 46414 Rhede/Westf., Gutenbergstr. 2, Alemania, declara que este producto está conforme con las Directivas de la UE enumeradas a continuación:
EN 61558-2-6:1997
EN 61558-1: 1997 +A1
Descripción del producto: Biological-/ Stereo-type microscope
Modelo/Denominación: BRESSER BioDiscover
Rhede, Julio 2007
Bresser GmbH
Helmut Ebbert
Gerente
DE GARANTIE & SERVICE
El período regular de garantía es dos anos iniciándose en el día de la compra. Para beneficiarse de un período de garantía más largo y voluntario tal y como se indica en la caja de regalo es necesario registrarse en nuestra página web.
Las condiciones de garantía completas así como informaciones relativas a la ampliación de la garantía y los servicios pueden encontrarse en www.bresser.de/warranty_terms. ¿Desearía recibir unas instrucciones de uso completas sobre este producto en un idioma determinado? Entonces visite nuestra página web utilizando el siguiente enlace (código QR) para ver las versiones disponibles.
O envíenos un mensaje a la dirección de correo manuals@bresser.de o déjenos un mensaje telefónico en el siguiente número +49 (0) 28 72 - 80 74-220*. Asegúrese de dejar su nombre, dirección, teléfono válido, una dirección de correo electrónico así como el número del artículo y su descripción.
*Número local de Alemania (el importe de cada llamada telefónica dependen de las tarifas de los distribuidores); Las llamadas des del extranjero están ligadas a costes suplementarios.


BRESSER
Bresser GmbH
Gutenbergstr. 2 · DE-46414 Rhede · Germany
Queda reservada la posibilidad de incluir modificaciones o de que el texto contenga errores.